Ali je dovoljeno igrati Boga?
Dr. Andrea Bannert je zjem od leta 2013. Doktor biologije in urednik medicine je sprva opravil raziskave v mikrobiologiji in je strokovnjak skupine za drobne stvari: bakterije, viruse, molekule in gene. Dela tudi kot svobodnjak za Bayerischer Rundfunk in različne znanstvene revije ter piše fantazijske romane in otroške zgodbe.
Več o strokovnjakihja Vse vsebine preverjajo medicinski novinarji.Prvič je bilo mogoče uspešno popraviti gensko spremembo pri človeških zarodkih. Toda s tehnologijo ni mogoče pozdraviti samo bolezni. Barvo oči in druge lastnosti bi lahko na ta način vnaprej določili. Bo kmalu prišel tudi oblikovalec?
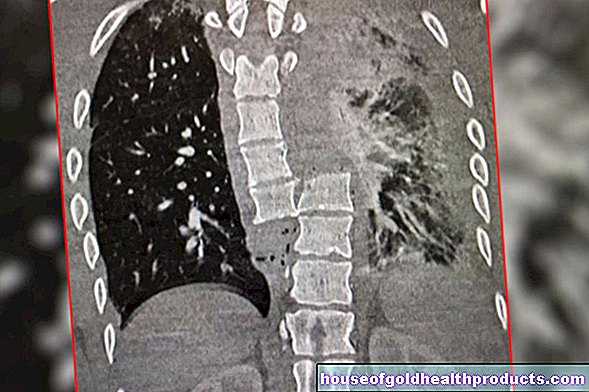
Simon K. * se je med vadbo zgrudil in se nikoli več ni zbudil. Diagnoza: nenadna srčna smrt. Mladi, atletski moški je trpel za tako imenovano hipertrofično kardiomiopatijo ali na kratko HCM. Pri tej bolezni se tkivo srčne mišice v levem prekatu zgosti. Motnja je relativno pogosta. Eden od 500 ljudi je prizadet in mnogi zaradi tega umrejo.
Škarje iščejo voditelje
Posebnost HCM: Podatki, tako imenovana genetska koda, se v enem trenutku spremenijo v zelo specifičnem genu. Znanstveniki temu pravijo mutacija. Obstaja približno 10.000 drugih dednih bolezni, ki jih sprožijo mutacije, ki so podobno izolirane. Cistična fibroza ali anemija srpastih celic - dve enako življenjsko nevarni bolezni. Očitna ideja je, da se resne genetske napake čim prej odpravijo.
Do nedavnega nemogoč podvig. Znanstveniki poznajo encime, ki lahko "razrežejo" DNK, vendar te proteinske molekule ne govorijo istega jezika kot genetske informacije. Zato ne morejo izslediti napake v genomu.
To se je spremenilo s spektakularnim odkritjem znanstvenikov Jennifer Doudna in Emmanuelle Charpentier pred štirimi leti. Po naključju so v bakterijah odkrili encim, ki lahko razreže verige DNK in s seboj kot tolmač nosi majhen delček genskega materiala. Lahko prebere ogromno podatkov v DNK in vodi molekularne škarje točno tam, kjer naj bi jih razrezali. Znanstveniki so poimenovali močno ekipo "CRISPR / Cas9" - bakterije jo potrebujejo za obrambo pred virusi.
Dedna bolezen se je zataknila v brstu
Skupina raziskovalcev z Univerze za zdravje in znanost Oregon v Portlandu je uporabila genske škarje za brisanje hipertrofične kardiomiopatije zelo zgodaj v genetski kodi - v zarodkih. Ekipa Shoukhrata Mitalipova je genske škarje opremila z genetskim zaporedjem, ki prepozna točno lokacijo v DNK, na kateri je programirana bolezen.
Svoje novo super orodje so uporabili pri 58 zarodkih, ki so nastali iz sperme moškega, ki trpi za HCM, in jajčnih celic zdrave ženske. Takšni poskusi so možni v ZDA. V Nemčiji pa zakon o zaščiti zarodkov preprečuje uporabo človeških zarodkov v raziskovalne namene.
Senzacionalna stopnja uspeha
Ameriški poskus je uspel: delček "tolmača" je vodil molekularne škarje Cas9 natančno do mutiranega segmenta DNA in ga ločil. Zdaj so lastni mehanizmi za popravilo celice lahko obnovili gen.
Uspeh je celo presenetil same znanstvenike: patogena mutacija je izginila pri 42 zarodkih - 72 -odstotna uspešnost.
"V celičnih kulturah pa CRISPR / Cas9 dolgo časa ni deloval tako dobro kot pri živih zarodkih," pravi Jun Wu, eden od avtorjev študije. Raziskovalci sumijo, da so razlog za to še posebej dobro delujoči stroji za popravljanje DNK v zgodnjih embrionalnih fazah.
Tudi prejšnji poskus kitajskih znanstvenikov aprila 2015 je deloval precej slabše od poskusa ameriških raziskovalcev. Za razliko od Mitalipova in njegove ekipe so Kitajci oplojenem jajčecu s svojim tolmačem dodali genske škarje - in ne v času oploditve.
Škarje izven nadzora
Kitajski raziskovalci so se morali spoprijeti z drugo težavo, s katero Mitalipov poskus ni naletel: tako imenovane mutacije izven cilja. Štejejo za največjo nevarnost pri uporabi CRISPR / Cas9.
Izven cilja pomeni, da genske škarje režejo tudi na drugih mestih, razen na želenem. Z lastnimi popravili celice ni vse mogoče pravilno sestaviti. Nato se pojavijo nove mutacije, ki bi lahko na primer sprožile raka.
"Vozimo avto, ki ga še vedno gradimo."
S svojim poskusom so Mitalipov in sodelavci znova obudili etično razpravo o tem, ali je ljudem dovoljeno manipulirati z zarodki. V Nemčiji je doslej dovoljena le tako imenovana diagnoza pred implantacijo. To vključuje pregled genetskega materiala zarodkov po umetnem oploditvi zunaj maternice in samo z uporabo zdravih zarodkov - torej tistih, ki nimajo resne dedne bolezni, kot je HCM. Metodo je mogoče uporabiti le, če obstaja grožnja resne dedne bolezni.
Tehnika CRISPR / Cas9 lahko ozdravi tudi tiste zarodke, ki bi bili izbrani med diagnostiko pred implantacijo. Teoretično. Ker je res bolje, bomo še videli. Tveganja, povezanega z zdravljenjem genskih škarij, še ni mogoče dokončno oceniti - znanstveniki se s tem strinjajo. Jacob Corn, direktor pobude za genomiko na kalifornijski univerzi v Berkeleyju, je o raziskovalnem statusu CRISPR / Cas9 dejal: "Vozimo avto, ki ga še gradimo."
Neznane nevarnosti
Enajst večjih ameriških znanstvenih organizacij v American Journal of Human Genetics poziva k "previdnemu, a predanemu pristopu". Dokler ne veste, ali koristi res odtehtajo tveganja. Raziskovalci zato menijo, da je "trenutno neprimerno" vstaviti gensko spremenjeni zarodek iz ženske in prinesti nosečnost.
Zarodki CRISPR / Cas iz poskusa Mitalipova so bili po nekaj dneh uničeni. V tem trenutku je zarodek sestavljen iz majhne, s tekočino napolnjene celične kroglice, blastociste. Znanstveniki te embrionalne faze še ne opredeljujejo kot človeško življenje. Če se blastocista ne vsadi v maternico, se iz nje v laboratoriju ustvarijo "samo" embrionalne izvorne celice.
Vprašanje, kdaj se življenje začne, je seveda mogoče argumentirati. V Nemčiji lahko na primer zarodke zamrznemo le v tako imenovani pronuklearni fazi in za namen umetnega oploditve ter jih na neki točki uničimo. Pri njih se jedro jajčne celice še ni popolnoma zlilo s semenom. Mnogi raziskovalci pozivajo k uporabi takšnih struktur za raziskovalne cilje na visoki ravni.
Dizajnerski dojenčki?
Kako daleč pa lahko greste pri genetskih raziskavah in terapiji? Odkritelj CRISPR / Cas9 Doudna je zaskrbljen in pravi: "Pogosto sem se vprašal, kaj bi raziskovalci naredili s to tehnologijo, za obstoj katere sem delno odgovoren jaz." Morda bi ustvarili oblikovalskega otroka, za katerega starši ne odločajo le o zdravju , pa tudi določiti barvo las, barvo oči, inteligenco in značaj - če takega poskusa zakon ne prepreči vnaprej. Skrajni čas je, da ugotovimo, katera tveganja lahko raziskovalci prevzamejo pri genski modifikaciji zarodkov in katere manipulacije bi načeloma morali prepovedati.
* Ime je spremenil urednik.
Tags.: Baby Child zobozdravstveno oskrbo anatomija






-infektion.jpg)
-maskenparty-in-der-schule.jpg)